轻松准确分剂量 | 助力儿童给药-酒石酸美托洛尔
将乐宜配和美托洛尔片通过一定的方法调制成混悬液,对该混悬液的含量,有关物质,溶出度和生物等效性进行评估。
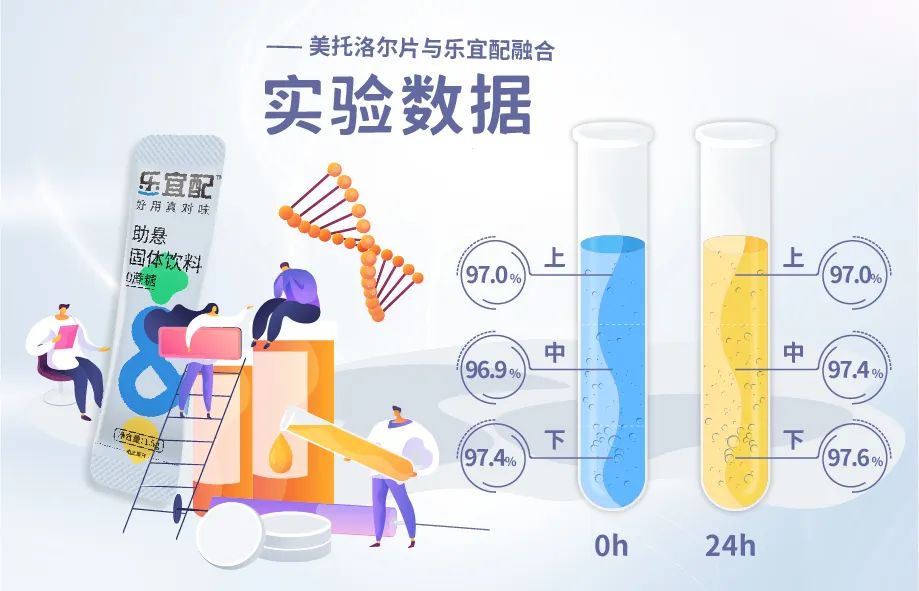
室温储存24h,质量稳定,符合中国药典片剂质量标准,同时体外溶出曲线考察表明,该混悬液与美托洛尔片有相似的溶出曲线,根据对酒石酸美托洛尔体内吸收特征的评估,可以认为调制美托洛尔混悬液与美托洛尔片具有生物等效性。
该项研究解决了美托洛尔片
用药的分剂量难题,
对儿童用药具有现实意义。
酒石酸美托洛尔是一种选择性β-1肾上腺素受体阻断剂。1975年4月18日,酒石酸美托洛尔片由阿斯利康公司开发在瑞典上市,规格为50mg和100mg。主要用于治疗高血压、心绞痛、心肌梗死等疾病,国内上市最低规格为25mg。
中文说明书未明确说明儿童用法用量,但是酒石酸美托洛尔片儿童用药在各医院广泛应用且分剂量医嘱占比高。酒石酸美托洛尔片市售最低剂量为25mg,没有酒石酸美托洛溶液剂上市。如何有效实现美托洛尔片的准确分剂量是医药界急需解决的问题。

鉴于以上现存问题,我们以临床需求为出发点,旨在解决目前儿童用药困难,开发了乐宜配产品用于调制口服固体制剂,并以CDE在2020年12月31日发布的《儿童用药(化学药品)药学开发指导原则》为依据,考察了乐宜配调制美托洛尔混悬剂的质量研究和生物等效性风险评估。
01
/
调制酒石酸美托洛尔
混悬剂的制备
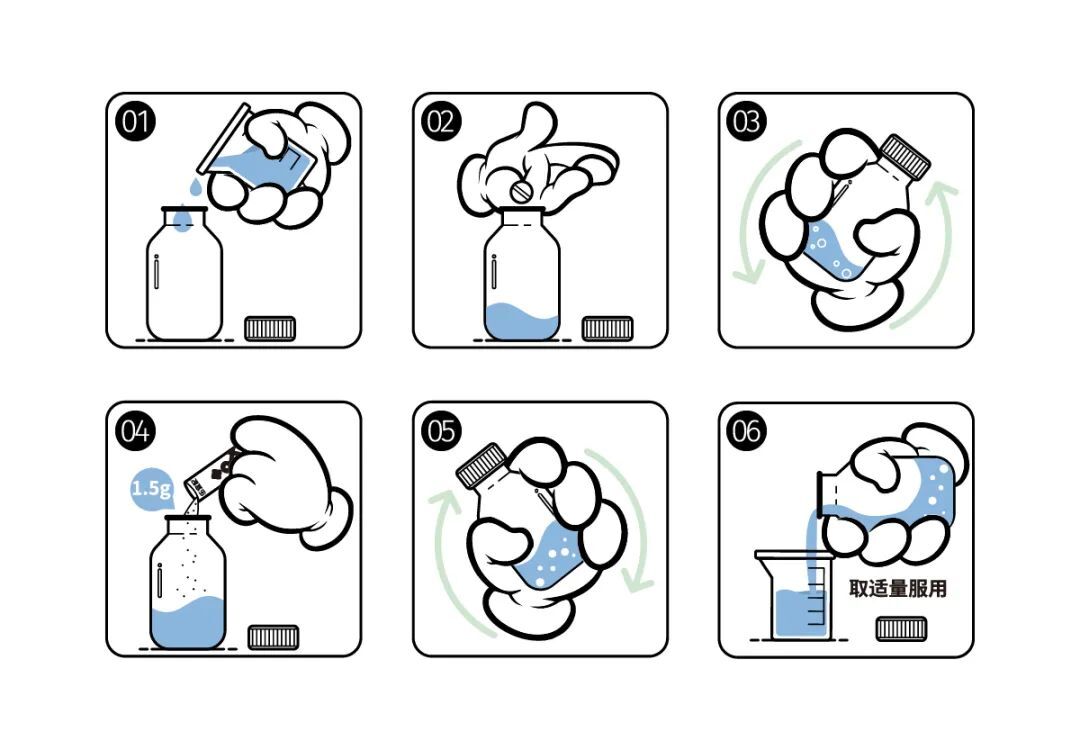
向30ml的PET瓶中加入9ml水,加入1片美托洛尔片(规格:25mg),磁力搅拌器1500rpm搅拌5分钟至完全崩解,加入乐宜配1.5g,再搅拌30s至均匀分散(加入乐宜配后,溶液体积溶胀至约10ml )得到2.5mg/ml调制美托洛尔混悬液。
02
/
调制酒石酸美托洛尔
混悬剂的质量研究
含量:调制美托洛尔混悬液室温储存0h~24h,含量均在标示量的95.0%~105.0%,且与配制混悬液前的片剂含量相似,满足市售片剂的含量标准,上、中、下含量的相对标准偏差小于5.0%,混悬剂含量均匀度合格(表1)。
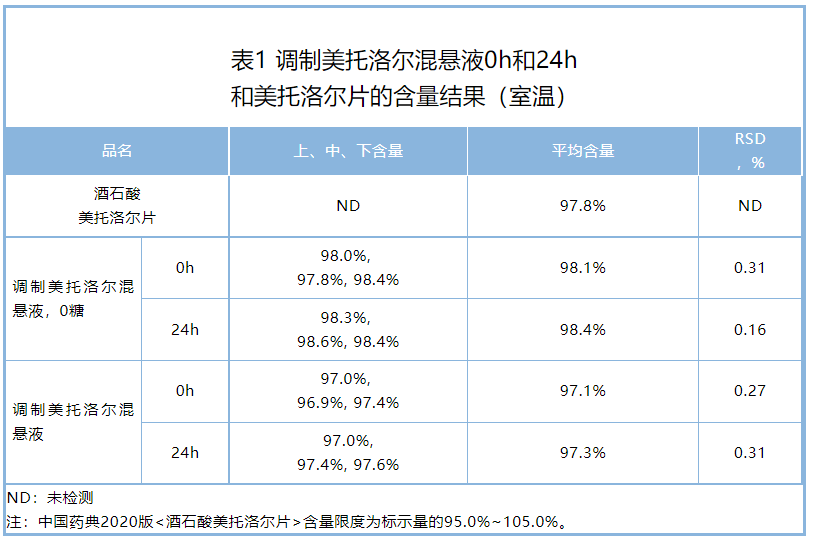
有关物质:乐宜配美托洛尔混悬液室温储存0h~24h,最大单杂均小于0.3%,总杂小于0.5%,满足市售片剂的有关物质标准(表2)。
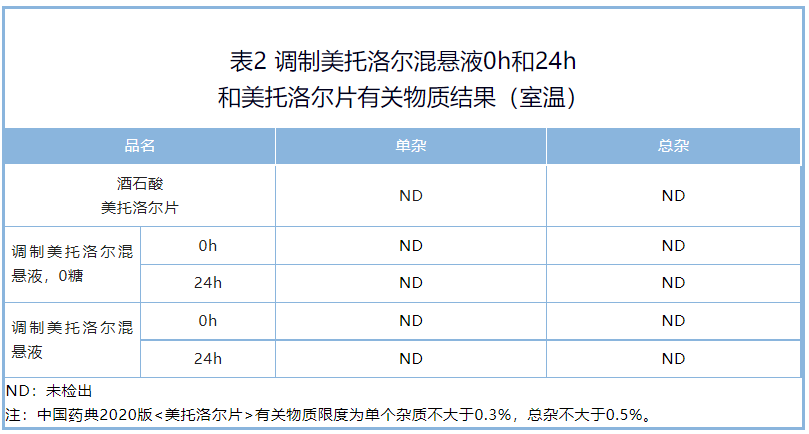
溶出度:乐宜配美托洛尔混悬液的溶出曲线与美托洛尔片溶出度在15分钟均大于85%,因此,根据溶出曲线比较指导原则,乐宜配美托洛尔混悬液与美托洛尔片具有相似的溶出曲线,且30分钟放行点(Q)大于75%,满足2020年版《中国药典》片剂溶出度标准(表3)。
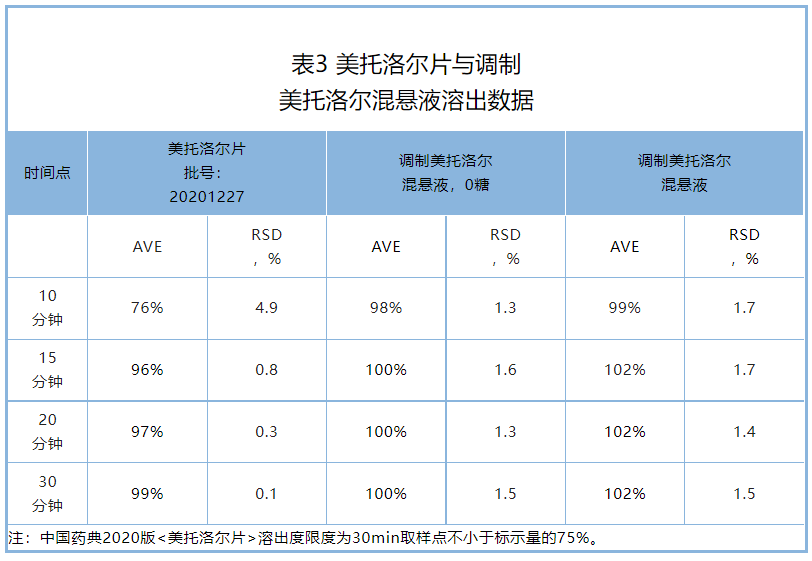
03
/
调制酒石酸美托洛尔
混悬剂生物等效性
风险评估

酒石酸美托洛尔在pH1.2、pH4.0、pH6.8和水中的溶解度均大于1.0g/ml,生理pH环境中溶解度很高,酒石酸美托洛尔生物药剂学分类列为BCSI类,属于高溶解,高渗透药物,酒石酸美托洛尔口服几乎完全被吸收,但是由于其广泛的首过效应,生物利用度大约为40%。
文献报道,改变处方的微晶纤维素、羧甲基淀粉钠和硬脂酸镁的量(控制在SUPAC-IR 2类变更),体内仍然与原研制剂生物等效,即使溶出度最慢的处方,如30min溶出度不符合USP标准,但是该处方体内仍然与原研制剂等效,因此对于2类变更的高溶解和高渗透药物的酒石酸美托洛尔片不需要生物等效性研究。

另一方面,酒石酸美托洛尔片被CDE列为可豁免生物等效性研究品种。
乐宜配所使用辅料在食品和药品中广泛应用,不含有山梨醇,甘露醇,聚乙二醇等影响药物吸收的辅料。综合评价,可以认为乐宜配调制美托洛尔混悬液与美托洛尔片具有生物等效性。
04
/
小结

本文结果显示,乐宜配和美托洛尔片配制的混悬液,含量均匀,室温储存24h,质量稳定,酸中体外溶出曲线与片剂相似,根据对美托洛尔体内吸收特性的评估,可以认为调制混悬液和美托洛尔片具有生物等效性。
乐宜配调制美托洛尔混悬液在临用前由患者家属自行调制,从配制液体中取部分服用,可以达到灵活调整剂量的目的,又可避免药物降解,具有很好的安全性,有效性和方便性。

用乐宜配调制美托洛尔混悬液
可准确的对美托洛尔片进行分剂量
药学研究符合《儿童用药(化学药品)药学开发指导原则》的要求,解决了美托洛尔片分剂量的难题,值得应用推广。
